O oxigênio líquido apresenta surpreendentemente propriedades magnéticas, que não podem ser explicadas por sua estrutura de Lewis. Esse fato levou à proposição de uma nova teoria para explicar ligações químicas.
Segundo a teoria dos orbitais, as ligações covalentes são formadas a partir da interpenetração dos orbitais atômicos. Esta interpenetração leva à formação de orbitais moleculares.
Considerando uma molécula de O₂, cujos núcleos atômicos estão localizados ao longo do eixo y, assinale a afirmação correta.
(Dado: número atômico do oxigênio = 8)
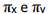 e uma ligação sigma
e uma ligação sigma 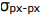
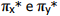 e uma ligação sigma
e uma ligação sigma 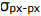
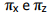 e uma ligação sigma σpy-py.
e uma ligação sigma σpy-py.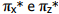 e uma ligação sigma σpy-py.
e uma ligação sigma σpy-py.