CONSTANTES

Constante de Avogadro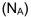 = 6,02 x 10²³ mol-¹
= 6,02 x 10²³ mol-¹
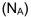 = 6,02 x 10²³ mol-¹
= 6,02 x 10²³ mol-¹Constante de Faraday (F) = 9,65 x 10⁴ °C mol-¹ = 9,65 x 10⁴ A s mol-¹ = 9,65 x 10⁴ J V-¹ mol-¹
Carga elementar = 1,60 x 10-¹⁹ C
Constante dos gases (R) = 8,21 x 10-² atm L K-¹ mol-¹ = 8,31 J K-¹ mol-¹ = 1,98 cal K-¹ mol-¹
Constante de Planck (h) = 6,63 x 10-³⁴ J s
Velocidade da luz no vácuo = 3,0 x 10⁸ m s-¹
Número de Euler (e) = 2,72
DEFINIÇÕES
Presão: 1 atm = 760 Torr = 1,01325 x 10⁵ N m-² = 1,01325 bar
Energia: 1 J = 1 N m = 1 kg m² s-² = 6,24 × 10¹⁸ eV
Condições normais de temperatura e pressão (CNTP): 0 °C e 1 atm, equivalente a um volume de um gás ideal de 22,4 L.
Condições ambientes: 25 °C e 1 atm
Condições padrão: 1 bar; concentração das soluções = 1 mol L-¹ (rigorosamente: atividade unitária das espécies); sólido com estrutura cristalina mais estável nas condições de pressão e temperatura em questão.
(s) = sólido. (l) = líquido. (g) = gasoso. (aq) = aquoso. (conc) = concentrado. (ua) = unidades
arbitrárias. u.m.a = = unidade de massa atômica. [X] = concentração da espécie X em mol L-¹
ln X = 2,3 log X;
Log 2 = 0,30
EPH = eletrodo padrão de hidrogênio
MASSAS MOLARES

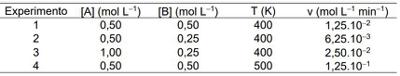
Os dados da tabela abaixo foram obtidos em um estudo de determinação dos parâmetros cinéticos de uma reação hipotética e irreversível do tipo A + B → C + D.

Não havendo mudança no mecanismo da reação no intervalo de temperatura considerado, determine os seguintes valores numéricos:
a) Ordem da reação em relação ao reagente A.
b) Ordem da reação em relação ao reagente B.
c) Ordem global da reação.
d) Constante de velocidade da reação a 400 K, com sua respectiva unidade de medida.
e) Constante de velocidade da reação a 500 K, com sua respectiva unidade de medida.
f) Energia de ativação da reação, em kcal mol⁻¹.